Die Wissenschafter aus St. Petersburg haben die antiviralen Eigenschaften von NSC 631570 in ihren Arbeiten mit Hepatitis C benutzt. Sie konnten zeigten, dass NSC 631570 in der optimal gewählten Dosierung bei 40 von 56 Patienten (80%) die Eliminierung des Virus aus dem Blut bewirkte (165).
In ihrer weiteren Studie haben die Forscher dieser Gruppe die klinische Anwendung von NSC 631570 in verschiedener Dosierungen mit dem rekombinanten humanen Interferon-alpha-2b (IFN) bei 75 Patienten mit chronischer Hepatitis C verglichen. Die besten Ergebnisse wurden mit NSC 631570 in der Einzeldosis 1 mg erzielt (203).
In einigen Publikationen wird potentielles Nutzen der Behandlung mit NSC 631570 bei AIDS diskutiert. Die Autoren schreiben, zum Beispiel, über verbesserte immunologische Parameter nach der Therapie (103).
Die antiviralen und insbesondere antigrippalen Eigenschaften von NSC 631570 wurden in Experimenten in vivo bestätigt (42, 51, 52, 88, 90).
NSC 631570 unterdrückt die Neubildung von Blutgefäßen, die einen Tumor versorgen. Dank dieser antiangiogenischen Eigenschaften bewirkt die präoperative Gabe von NSC 631570 eine bessere Abgrenzung der Tumore vom gesunden Gewebe und die Tumorabkapselung. Dies erleichtert die chirurgische Entfernung des Tumors, was in den Universitätsstudien bei Brustkrebs belegt wurde (68-73, 114). Es wird empfohlen, die Tumorlast 7-10 Tage nach Therapiebeginn nach Möglichkeit chirurgisch zu reduzieren.
In Laborversuchen hat NSC 631570 die Vermehrung der menschlichen Endothelzellen auf dosis-abhängige Weise unterdrückt, ohne dabei die zytotoxischen Eigenschaften zu realisieren. Am Modell der Kapillarenbildung wurde die Inhibierung von Angiogenese beobachtet. Die tumorale Angiogenese ist die Neubildung von Gefäßen, die einen wachsenden Tumor mit Nährstoffen versorgen und welche von kritischer Bedeutung für das Tumorwachstum sind (136).
Hemmung der Sprossen durch NSC 631570 (NSC 631570) im endothelialen Sphäroid-Modell

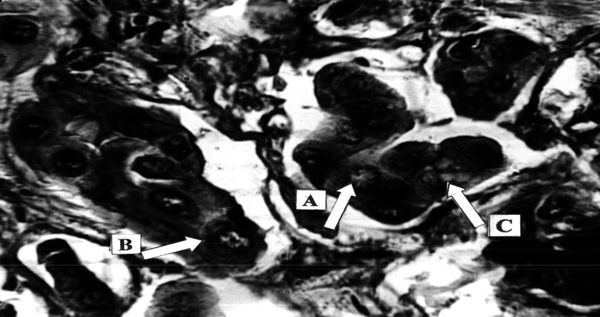
Bauchspeicheldrüsen-Adenokarzinom. Präoperative Behandlung mit NSC 631570, insgesamt 100 mg, 10 Tage vor der Operation (Pankreas-Duodenektomie=Bauchspeicheldrüsen-Zwölffingerdarmentfernung). Bildung einer Kapsel (A) rund um den Tumor. Die Krebszellen dringen in diese Kapsel nicht ein. Massive Infiltration von Rundzellen an der Grenze der Tumorkapsel. H-e, x100.

Pancreatisches Adenokarzinom. Präoperative Behandlung mit NSC 631570, Gesamtdosis 100 mg, 10 Tage vor der Pankreatikoduodenektomie. Tumornekrose (A), Inhibierung der Neugefäßbildung (Defekt in der Kapillarwand, Defekt in der Endothelschicht, B). H-e, x200.
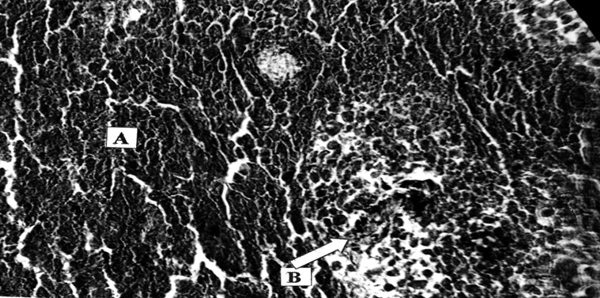
Pancreatisches Adenokarzinom. Präoperative Behandlung mit NSC 631570, Gesamtdosis 100 mg, 10 Tage vor der Pankreatikoduodenektomie. Tumornekrose (A), Inhibierung der Neugefäßbildung (Defekt in der Kapillarwand, Defekt in der Endothelschicht, B). Zellkernveränderungen: Chromatindispersion (A) und -fragmentierung (B), hydropische Degeneration im Zytoplasma (C). Eisen-Hematoxylin – van Gieson, x500.
DIE UNTERSUCHUNGEN IN VITRO
Die klinisch beobachtete Wirksamkeit von NSC 631570 ist kein Zufall oder gar „spontane Selbstheilung“ sondern eine Folge der Wirkungsmechanismen von NSC 631570, die in zahlreichen Laborversuchen in vitro und in vivo nachgewiesen wurden. Bis heute wurde NSC 631570 an mehr als 100 Krebszelllinien und auch an gesunden Zellen getestet.
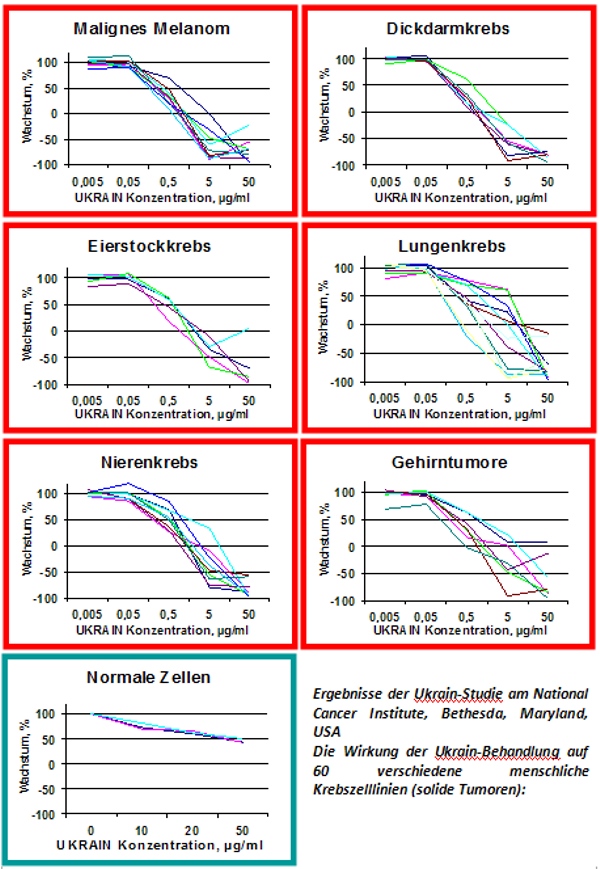
Unter anderem ist NSC 631570 in den Zellstudien an National Cancer Institute (Bethesda, Maryland, USA) an 60 Zelllinien geprüft worden, welche acht wichtige menschliche bösartige Tumore vertreten: Hirntumor, Eierstockkrebs, kleinzelliges und nichtkleinzelliges Bronchialkarzinom, Dickdarmkrebs, Nierenkrebs, Leukämie und Melanom. NSC 631570 war gegen alle diese Zelllinien toxisch wirksam (40, 190). Im Vergleich zu 5-Fluorouracil (5-FU) und Gemcitabine, zwei Standardzytostatika zur Behandlung von Karzinomen der Verdauungsorgane, erreichte NSC 631570 bessere Ergebnisse. Bei diesen Versuchen hat es nicht nur das Zelllinienwachstum gehemmt sondern auch die Krebszellen abgetötet.
Ergebnisse der Ukrain-Studie am National Cancer Institute, Bethesda, Maryland, USA
NSC 631570 bewirkte für beinahe alle Krebszelllinien Wachstumshemmung zwischen 50% und 100%, welche sich bei höheren Konzentrationen (50 µg/ml) in einen zytolytischen Effekt verwandelte, der die Reduktion der gesamten Zellmasse bewirkte. Die höchste Konzentration von NSC 631570 (50 µg/ml) hemmte die Vermehrung von normalen Zellen (Endothelzellen, Fibroblasten, Keratinozyten, Prostata-Epithelzellen) ohne jeglichen zytotoxischen Effekt. Das Chemotherapeutikum 5-Fluorouracil (NSC 19893), welches unter den gleichen Bedingungen untersucht wurde, hemmte das Wachstum vollständig nur bei einigen wenigen Linien mit extrem hohen Konzentrationen (500 µg/ml), während eine Reduktion der Zellmasse niemals beobachtet wurde.
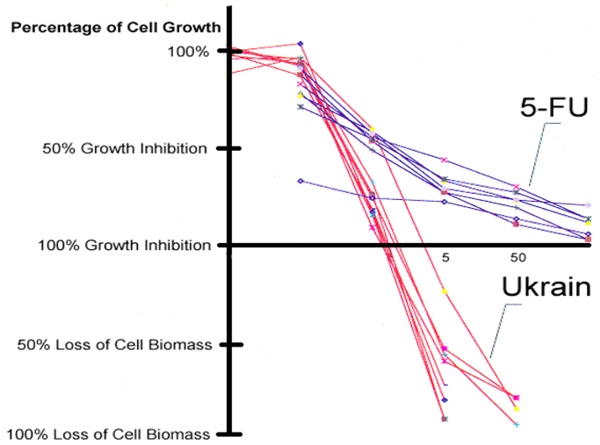
Vergleich der Toxizität von NSC 631570 (NSC 631570) und 5-Fluorouracil (NSC 19893) gegen verschiedene Krebszelllinien.
Die zytostatische Wirkung von NSC 631570 auf die Krebszelllinien M-HeLa und Hep-2/0-6-5 war stärker ausgeprägt im Vergleich zum synthetischen Präparat Oliphen (61).
Im Experiment hat NSC 631570 das Wachstum von vier Ewing-Sarkomzelllinien auf zeit- und dosisabhängige Weise gehemmt. In diesen Versuchen war seine Wirkung stärker ausgeprägt als jene von Thiotepa (243, diskutiert in 244).
In einer Arbeit an Ehrlichschen Karzinomzellen und Lympholeukemie P-388 haben die Autoren gezeigt, dass die Empfindlichkeit der malignen Zellen zu NSC 631570 stark von der Zellzyklusphase abhängt, wobei das erste Maximum der Empfindlichkeit auf das Ende der Phase G1 fällt und das zweite – auf die Phase G2 (148).
In einer Studie wurde der Einfluss von Glukose, Bernsteinsäure, pH-Wert und erhöhter Temperatur auf die Wirksamkeit von NSC 631570 gegen Krebszellen in vitro untersucht. Glukose verminderte die zytotoxische Wirkung von NSC 631570, Bernsteinsäure verstärkte sie. Am stärksten war die Wirkung bei pH 7,3-8,0, und die Temperatur von 41,5 C hatte keinen Einfluss auf die Wirkung von NSC 631570 (117).
Selektive Wirkung von NSC 631570
In Vergleichsstudien wurde NSC 631570 an 18 bösartigen und 12 normalen Zelllinien unter identischen Bedingungen getestet (36, 38, 63, 143, 147, 149, 181, 184, 190, 245, 255). Diese Experimente haben alle Zweifel hinsichtlich der selektiven Wirkung von NSC 631570 aufgeräumt. Die zahlreichen Arbeiten haben bewiesen, dass NSC 631570 das erste und einzige Krebsmedikament ist, das toxisch für Krebszellen, jedoch nicht für gesunde Zellen ist. Das erklärt auch seine gute Verträglichkeit bei klinischer Anwendung.
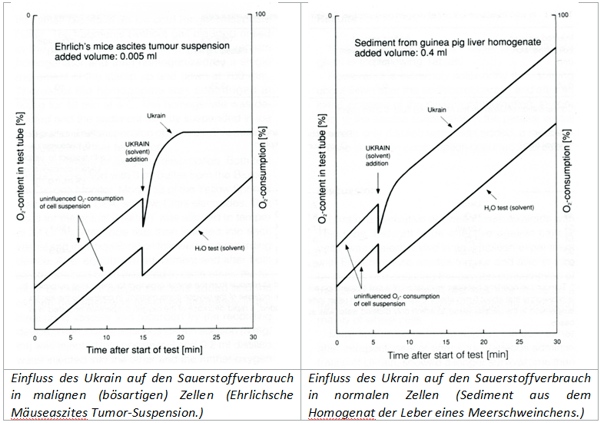
Erste Hinweise auf die selektive Wirkung von NSC 631570 auf Krebszellen lieferte eine frühe Studie aus dem Jahre 1976 von der Bundesstaatlichen Anstalt für Experimentell-Pharmakologische und Balneologische Untersuchungen, welche einen unterschiedlichen Sauerstoffverbrauch durch normale Leberzellen und aszitische Zellen des Ehrlichschen Tumors nach der Inkubation mit NSC 631570 feststellte (38).
Etwa zur selben Zeit haben die Forscher der Wiener Universität für Bodenkultur die hemmende Wirkung von NSC 631570 auf die Vermehrung von bösartigen und normalen Zellen verglichen. Um eine 50%-Wachstumshemmung zu erreichen, musste bei normalen endothelialen Zellen eine zehnfache Konzentration von NSC 631570 im Vergleich zu einer menschlichen Osteosarkomzelllinie verwendet werden. Laserabtastungsmikroskopie zeigte ein hohes Aufnahmevermögen von NSC 631570 in bösartigen Zellen, während die Aufnahme in normalen Zellen unter denselben experimentellen Bedingungen wesentlich niedriger war (36).
Der unterschiedliche Einfluss von NSC 631570 auf den Sauerstoffverbrauch in gesunden Zellen und Krebszellen
Die Aufnahme von NSC 631570 in Melanom-Zellen, verglichen mit normalen Zellen (in vitro)

Ref: Hohenwarter O. et al. “Selective inhibition of in vitro cell growth by the anti-tumour drug Ukrain” Drugs under Experimental Research (1992) S.1-4 (36)
Diese selektive Wirkung von NSC 631570 auf die Krebszellen wurde in zahlreichen Studien an renommierten Universitäten und Forschungseinrichtungen bestätigt.
In der Studie der European Organisation for Research and Treatment of Cancer (EORTC) wurden die Zellen der humanen Tumorxenograften (HTX) den Nacktmäusen transplantiert. Weiter wurden diese Tumorzellen mit verschiedenen Konzentrationen von NSC 631570 inkubiert. Folgende HTX wurden verwendet: Dickdarmkrebs CXF 1103/11, Magenkrebs GXF 217/17, Bronchialkarzinom LXFL 529/14, Brustkrebs MAXF 401/13, Melanom MEXF 276/10 und Eierstockkrebs OVXF 899/9. NSC 631570 war aktiv gegen OVXF 899/9 bei 10 µg/ml und in allen getesteten Kolonien bei 100 µg/ml mit der T/C-Verhältnis („test to control“) 1/135 bei OVXF, 8/109 bei CXF, 10/98 bei GXF, 15/187 bei LXFL, 34/133 bei MAXF und 10/122 bei MEXF (64, 189).
Beim 89. jährlichen Treffen der Amerikanischen Gesellschaft für Krebsforschung (American Association for Cancer Research) in New Orleans, USA im Jahre 1998 präsentierten die Wissenschafter der University of Pretoria, Südafrika die Ergebnisse ihrer Arbeit über selektive Wirkung von NSC 631570 an verschiedenen Krebszelllinien. Die Autoren stellten fest, „dass NSC 631570 für Krebszellen selektiv toxisch ist, indem es einen Metaphasenblock verursacht, der durch eine anomale Chromosomenverteilung charakterisiert wird und auf die Bildung von Mikrokernen und in Apoptose hinausläuft“ (139). Diese Forschungsgruppe hat 2000 entdeckt, dass NSC 631570 die Polymerisation von Tubulin hemmt (140).
Wissenschafter der Eberhard-Karls-Universität (Tübingen, Deutschland) untersuchten den Effekt von NSC 631570 auf das Zellüberleben, die Modifizierung des Zellzyklus und die Induktion der Apoptose ohne und in der Kombination mit Bestrahlung. NSC 631570 modulierte die Schädlichkeit der Bestrahlung auf menschliche Tumorzelllinien und schützte normale Zellen vor den Strahlen. Die Kombination von NSC 631570 mit ionisierenden Strahlen verstärkte die Toxizität gegenüber den Krebszelllinien CCL-221 und U-138MG, aber nicht gegenüber den MDA-MB-231 und PA-TU-8902. Eine strahlenschützende Wirkung wurde gegenüber den normalen menschlichen Haut- und Lungenfibroblasten gefunden (184).
Die zytotoxische Wirkung von NSC 631570 wurde in zwei primären Bauchspeicheldrüsen-krebszelllinien (PPTCC), Fibroblasten aus duktalen Pankreaskarzinomgewebeproben (F-PDAC) und einer immortalisierten duktalepithelialen Pankreaszelllinie (HPNE) untersucht. Die Zytotoxizität wurde mittels CellTiter 96-Satz erfasst. Die Methode basiert auf dem Zellmetabolism der Tetrasoliumsubstanz XTT, welche von lebenden Zellen reduziert wird um ein lösliches Formazanprodukt beim Vorhanden der Elektronen-ankoppelnden Substanz Phenazinmethosulfat zu bekommen. Modulierung der NSC 631570-Aufnahme im Nährboden wurde mithile von Fluoreszenz von NSC 631570 mit AlphaDigiDoc-Software im UV-Licht bestimmt. Die zytotoxische Wirkung von NSC 631570 in PPTCC war wesentlich höher als in F-PDAC- und HPNE-Zellen (20% gegen 80% lebende Zellen). Außerdem hat der Fluoreszenz-Test ergeben, dass PPTCC-Zellen mehr Präparat aufgenommen haben als F-PDAC- und HPNE-Zellen. Diese Ergebnisse zeigen selektive Wirkung von NSC 631570 in den PPTCC-Zellen, was auf verschiedene Transportsysteme oder auf eine höhere Metabolismrate des Präparates in den PDAC-Zellen, und befürworten weitere Studien über mögliche Rolle von NSC 631570 in der Behandlung von Pankreaskarzinomen (265).
Induktion der Apoptose in den Krebszellen
In der Studie über die Wirkung von NSC 631570 auf die Erythroleukemiezellen K-562 wurde gefunden, dass dieses Präparat einen bimodalen Krebszellentod bewirkt. Bei niedrigeren Konzentrationen von NSC 631570 sterben die malignen Zellen infolge Apoptose ab, bei höheren Konzentrationen wird die Mikroröhrchenbildung verhindert und Polyploidie entsteht (56, 62).
Die Forscher der Rochester University, USA haben gezeigt, dass NSC 631570 die Anhäufung von Prostatakrebszellen sowie Epidermoidkarzinomzellen in der G2M-Phase auslöste, nicht aber von normalen Zellen (149, 150).
Die Wissenschafter der University of Pretoria, Südafrika haben in den Versuchen an menschlichen Zervixkarzinomzellen HeLa, Plattenepithelkarzinom WHCO5, normaler Nierenzelllinie Graham 293 und transformierter Nierenzelllinie Vero von afrikanischem grünen Affen erforscht, dass NSC 631570 für Krebszellen selektiv toxisch ist, indem es einen Metaphaseblock verursacht, der durch eine anomale Chromosomenverteilung charakterisiert wird und auf die Bildung von Mikrokernen und in Apoptose hinausläuft (139).
Wissenschafter der Eberhard-Karls-Universität (Tübingen, Deutschland) untersuchten den Effekt von NSC 631570 auf das Zellüberleben, die Modifizierung des Zellzyklus und die Induktion der Apoptose ohne und in der Kombination mit Bestrahlung. Sie haben herausgefunden, dass die Kombination von NSC 631570 mit ionisierenden Strahlen die Toxizität gegenüber den Krebszelllinien CCL-221 und U-138MG verstärkte. Gleichzeitig schützte NSC 631570 die normalen menschlichen Haut- und Lungenfibroblasten vor den ionisierenden Strahlen (184).
Die tödliche Aktion des NSC 631570 (NSC 631570) gegen Krebszellen - Einsetzen der Apoptose
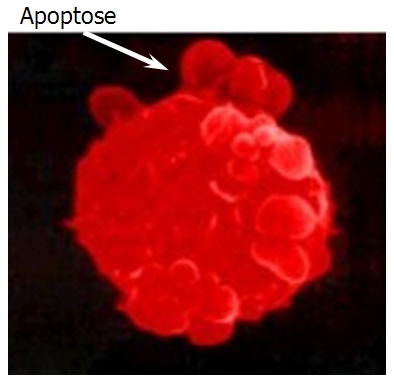
Bei Beurteilung der Zellproliferation nach der BrdU-Aufnahme in den Zelllinien AsPC1, BxPC3, MiaPaCa2, Jurkat und THP-1 und der Zellzyklusphasen – mit Hilfe von Giemsa-Färbung, haben die Autoren festgestellt, dass 10 µg/ml NSC 631570 nach 24 Stunden eine deutliche Ansammlung der Krebszellen in der Phase G2M bewirkt. Die Apoptoserate in den peripheren Mononuklearen war bei den ähnlich inkubierten und Kontrollzellen gleich. Außerdem zeigten mitogen-stimulierte Lymphozyten eine erhöhte blastogene Reaktion (181).
Die Induktion der Apoptose durch NSC 631570 wurde auch in den in vitro Versuchen an den Eierstockzellen der chinesischen Hamster bestätigt. In diesem Experiment waren die Wirkungen von NSC 631570 und Etoposid synergistisch (167).
Inhibierung der Polymerisation von Tubulin durch NSC 631570
In den Versuchen mit Tubulin aus dem Rinderhirn haben die Forscher der Pretoria University entdeckt, dass NSC 631570 die Polymerisation des Proteins Tubulin hemmt (146).
Der Wirkungsmechanismus von NSC 631570 bei Bauchspeicheldrüsenkrebs wurde an den Zelllinien AsPC1, BxPC3, Capan1, MiaPaCa2 und Panc1 erforscht. Dabei zeigte sich, dass NSC 631570 einen dosisabhängigen Zellzyklusstopp in der Phase G2M bewirkte. Serienversuche zeigten, dass die Wirkung von 10 µg/ml NSC 631570 auf die Zellzyklusphasen nach 8 Stunden Inkubation irreversibel war. Experimente mit Tubulinpolymerisation haben gezeigt, dass NSC 631570 die Tubulinmonomere stabilisiert und infolgedessen die Bildung von Mikrotubulinröhrchen hemmt (143).
Aktivierung der mitochondrialen Kaspasen
Caspasen sind die wichtigsten Enzyme der Apoptose, des programmierten Zelltods und spielen somit eine wichtige Rolle in den Mechanismen der Krebsbehandlung.
Die Fähigkeit von NSC 631570 die Apoptose zu induzieren wurde an einem Jurkat-Lymphoma-Model erforscht. NSC 631570 erwies sich als ein starker Apoptose-Induktor. Vertiefte Untersuchungen haben gezeigt, dass es Depolarisierung von mitochondrialen Membranen und als folge die Aktivierung von Caspasen hervorgerufen hat (246).
Caspasen bestehen aus zwei Klassen, Initiatoren und Effektoren. Die Initiator-Caspasen 8 und 10 führen die Todfaktor-abhängige, oder extrinsische Apoptose herbei, dahingegen vermittelt die Effektor-Caspase 9 die intrinsische oder mitochondriale Apoptose.
Forscher am Institut Nacional de Cancerologia, Mexiko City, Mexiko stellten fest, dass NSC 631570 in einer Reihe von Krebszelllinien (menschliche Zervixkarzinome HeLa, HeKB, HeKS32, HeBcll3, HeNFR und HelKK, Dickdarmkrebs SW480, Nierenkrebs HEK293, Osteosarkom MG 63) die Apoptose auslöst, indem es den inneren Zelltodweg aktiviert. Interessanterweise war die nichttransformierte Fibroblastenzelllinie hTERT diesem Medikament gegenüber unempfindlich (255).
Die Wirkung auf Cycline und Cyclin-abhängige Kinasen
Cycline sind Proteine, die eine Schlüsselrolle in der Steuerung des Zellzyklus spielen. Sie sind in der Lage, mit Cyclin-abhängigen Kinasen (CDK) Komplexe zu bilden sowie deren Kinasefunktion zu aktivieren. Da die Cyclinkonzentration im Gegensatz zur Konzentration der CDK zellzyklusabhängig reguliert ist, fungieren diese Proteine ihrerseits auch als Regulatoren der Cyclin-abhängigen Kinasen. Cycline können durch die Aktivierung verschiedener Cyclin-abhängiger Kinasen und einer damit verbundenen Phosphorylierung verschiedener Substrate eine Rolle in verschiedenen Teilen des Zellzyklus spielen. Steigende Konzentrationen von Cyclin A, z.B., leiten die Zelle in die G2-Phase, während Cyclin B für den Start der Mitose essenziell ist.
Die Forscher der Rochester University haben an den Epidermoidkarzinomzelllinien ME180 und A431 sowie Prostatakrebszelllinie LNCaP die Wirkung von NSC 631570 auf die Konzentrationen von Cyclinen und Cyclin-abhängigen Kinasen untersucht. Es wurden die Änderungen in den Konzentrationen von mitotischen Cyclinen A und B1 sowie CDK1 und CDK2 gefunden. Die Forscher haben auch eine erhöhte Expression des CDK-Inhibitors p27 in beiden Krebszelllinien beobachtet, was zur Anreicherung der Krebszellen, nicht aber von normalen Zellen in der G2/M-Phase führen kann (147, 149).
Die Wirkung von NSC 631570 auf die Expression von hENT1 und dCK
Die Wechselwirkungen zwischen NSC 631570 und den molekularen Determinanten hENT1 und dCK, welche am Metabolismus von Gemcitabin beteiligt sind, wurden in vitro an pankreatischen Adenokarzinomzelllinien (PDAZ) untersucht. Zwei ATCC Zelllinien PL45 und MiaPaCa-2 sowie zwei primäre Zelllinien PPTCC78 und PPTCC109 von Patienten mit PDAZ nach den Resektionen wurden verwendet. Die Zellen waren mit NSC 631570 im Konzentrationsbereich von IC50 für 48 Stunden behandelt. Alle Vervielfältigungen wurden nach der Normalisierung der Genexpression gegen das Glycerinaldehyd-3-phosphat-Dehydrogenase (GAPDH) Haushaltskontrollgen ausgeführt und die quantitative Bestimmung wurde durchgeführt. NSC 631570 in der Dosierung IC50 hat die Expression von hENT1-mRNA in allen PDAZ Zelllinien positiv moduliert (p<0,001). Die Analyse zeigte einen durchschnittlichen 2,8fachen Anstieg im Vergleich zu den unbehandelten Kontrollzellen (p=0,001). In den Zelllinien PL45 und MiaPaCa-2 hat NSC 631570 auch die mRNA-Expression vom dCK-Gen positiv beeinflusst (264).
Von den früheren klinischen Daten ausgehend, erscheint die Kombination von NSC 631570 und Gemcitabin als ein viel versprechendes Protokoll. Die Ergebnisse dieser experimentellen Studie liefern die experimentelle Grundlage für weitere klinische Studien mit dieser Kombination in den PDAZ-Patienten (Funel et al, ‘Molecular mechanisms underlying the synergistic interaction of the novel anticancer drug NSC 631570 with gemcitabine in preclinical models of pancreatic cancer’, 44th Annual Pancreas Club Meeting, New Orleans, USA 2010).
Die Wirkung von NSC 631570 auf DNS- und Proteinsynthese
Die Wirkung von NSC 631570 auf DNS- und Proteinsynthese in Krebszellen wurde in vitro erforscht. Es wurde gezeigt, dass NSC 631570 (1-100 µg/ml) eine Dosis abhängige Inhibierung der DNA-, RNA- und Proteinsynthese in Krebszellen bewirkt, was an einer Reihe von Zelllinien gezeigt wurde, einschließlich Mauslymphom, HeLa, Yoshida, Mausmyelom, menschliche WiDr-Tumor, EB, EsB, YAC-1 und P815. Bei gleichen Testbedingungen waren DNA-, RNA- und Proteinsynthese in normalen Zellen (menschliche Mandelzellen und Leberzellen des Meerschweinchens) viel weniger gehemmt (58, 63).
Unter vielen möglichen Mechanismen der Wirkung von NSC 631570 wurde auch sein Einfluss auf die Endonukleasen der Rattenleber und auf die Topoisomerasen – Enzymen, die in dem DNA-Stoffwechsel eine wichtige Rolle spielen, untersucht. NSC 631570 hat in diesen Versuchen sowohl die metallabhängigen Endonukleasen, als auch die Topoisomerase I inhibiert (166).
Die Wirkung auf Proteine, welche am Umbau der extrazellulären Matrix beteiligt sind
Eine italienische Forschungsgruppe von der Universität Mailand, verwendete RT-PCR, Western-Blot-Methode und SDS-Zymography, um die Wirkung von NSC 631570 auf die Expression von Genen und Proteinen zu untersuchen, welche am Umbau der extrazellulären Matrix beteiligt sind (dieser Mechanismus ist mit der Tumor-Invasion der menschlichen Glioblastomzellen verbunden). Es gab eine bedeutende dosisabhängige Abnahme in der Glioblastomzellproliferation und eine Tendenz zur Downregulation von SPARC („secreted protein acidic cysteine-rich“). Diese Studie lieferte die theoretischen Gründe für die Anwendung von NSC 631570 bei solchen Tumoren. Die Forscher fassten zusammen: NSC 631570 kann eine nützliche Therapie bei Gehirntumoren sein(245). Dies wurde bei klinischer Anwendung bestätigt (Siehe „Gehirntumore“).
In ihrer weiteren Arbeit mit Glioblastomzelllinien haben die italienischen Forscher festgestellt, dass NSC 631570 die Expression vom sauren Gliafaserprotein (GFAP) erhöht. Die Expression des Connexin 43 war von NSC 631570 nicht beeinflusst (250).
Die Wirkung von NSC 631570 auf die Modulierung einiger Schlüsselmarker der Tumorprogression in pankreatischen Karzinomen wurde an drei Zelllinien HPAF-II, PL45 und HPAC untersucht. Die Zelllinien wurden mit NSC 631570 (5, 10 and 20 µM) für 48 Stunden behandelt oder unbehandelt gelassen. Die mRNS von Secreted protein acidic and rich in cysteine (SPARC) wurden mittels Echtzeit-PCR bestimmt. Die Aktivitäten der Matrixmetalloproteinasen (MMP)-2 und -9 wurden mit SDS-Zymographie bemessen. Die Konzentrationen vom SPARC-Protein in Zelllysaten und Überständen wurden mittels Western blot bestimmt. Zellzyklus wurde mit Durchflusszytometrie und Invasion mit Matrigel-Invasionstest untersucht. NSC 631570 rufte Senkung von MMP-2 und MMP-9 hervor, was darauf hinweist, dass dieses Präparat die Invasion von Pankreaskrebszellen hemmen kann, was auch in Matrigel-Invasionstest bestätigt wurde. Die Inhibierung von SPARC in den Überständen spricht für die Inhibierung des extrazellulären Remodelling des Matrix in der Tumormikroumgebung. Gleichzeitig weist die Erhöhung von SPARC-mRNS und des Zellproteins darauf hin, dass NSC 631570 die Zellproliferation beeinflussen kann indem es einen G2/M-Block in den Zellen bewirkt (266).
Die Wirkung auf die Hitzeschockproteine
In den Experimenten mit den humanen Lymphomzellen wurde die Wirkung von NSC 631570 auf die Zelllinien U-937 und U-937/hsp70, welche sich in der Expression der Hitzeschockproteine unterscheiden. Es stellte sich heraus, dass die Linie U-937/hsp70 gegen die Wirkung von NSC 631570 mehr resistent war, was die Autoren auf die schützende Wirkung vom Hsp70 zurückführen (200).
Die Beeinflussung des elektrokinetischen Potentials
Es wurde untersucht, wie NSC 631570 das elektrokinetische Potential (EKP) von malignen und gutartigen Zellen beeinflusst. Das EKP der Ehrlichschen Karzinomzellen sank nach der Inkubation mit NSC 631570. Die Verminderung des EKP von normalen Thymozyten war weniger ausgeprägt (221).